细小病毒病原诊断方法及预防,犬细小病毒的诊断方法
细小病毒病原诊断方法及预防
犬细小病毒的诊断方法可根据血常规检测结果和疾病的主要症状进行临床初步诊断。血常规检查显示血细胞比容增加,白细胞计数正常或偏低。人们通常认为,被病毒感染的狗排出的带有番茄汁或酱油气味的血液是该疾病的特征性症状,可以作为初步诊断的基础。犬细小病毒胶通常用于犬细小病毒病的诊断。

猪细小病毒病的防治
这种疾病没有治愈的方法。 母猪在交配前可以通过自然感染和人工免疫获得主动免疫。 自然感染的方法是将一些血清阳性的成年母猪放入一群血清阴性的幼母猪中,幼母猪通过对成年母猪解毒而被感染 这种方法只适用于这种疾病的流行。猪细小病毒病是由细小病毒科猪细小病毒引起的猪繁殖障碍之一。这种疾病的主要特征是感染的母猪,特别是初产母猪,它们产生死胎、畸形胎儿、木乃伊胎、虚弱小猪和健康小猪。母猪没有明显的其他症状。 这种疾病发生在我国的许多养猪场,尤其是集约化养猪场。番鸭细小病毒病是由鸭细小病毒引起的急性感染,影响1-4周龄的雏番鸭。腹泻和气喘是该疾病的主要症状,其发病率和死亡率相对较高。近年来,番鸭病在我国福建、广东等省普遍存在,造成了极大的危害。 (1)临床症状该疾病大多是急性的。这种疾病的最初表现很好。[病原体]该病为鸭细小病毒引起的急性败血症感染,主要影响5-20日龄雏鸭。发病主要集中在2-4周龄的雏鸭。发病高峰是3周,所以被称为“三周脖子” 一旦疾病发生,它会在几天内影响整个群体。 [诊断] ①该病的主要症状是气喘、腹泻、脱水、脚软、迅速消瘦。番鸭细小病毒病只发生在2-4周龄的雏番鸭中,其他品种的雏鸭、鸡和鹅没有感染。临床表现为腹泻、呼吸困难和脚软。结合尸检变化,可以做出初步诊断。 为了作出明确的诊断,应取死番鸭的肝、脾或胰腺送兽医检验科进行实验室诊断。
犬细小病毒的诊断方法
犬细小病毒的诊断方法可根据血常规检测结果和疾病的主要症状进行临床初步诊断。血常规检查显示血细胞比容增加,白细胞计数正常或偏低。人们通常认为,被病毒感染的狗排出的带有番茄汁或酱油气味的血液是该疾病的特征性症状,可以作为初步诊断的基础。犬细小病毒胶通常用于犬细小病毒病的诊断。

猪细小病毒病的防治
细小病毒病原诊断方法及预防范文
本文的目录导航:
[标题]鸭细小病毒灭活疫苗的研制
[1.1-1.7]鸭细小病毒灭活疫苗研制简介
[1.8-1.11]细小病毒病原体诊断方法和病毒疫苗研制材料及方法
[第二章]新型鸭细小病毒疫苗的研究成果
[第四章-参考文献]鸭细小病毒灭活疫苗研制的讨论与结论
1.8病原诊断方法
对于鸭细小病毒的鉴定,初步需先对患病动物外貌、精神状态进行观察。然后,根据该病造成的临床症状和剖检病变,对动物进行初步判断。之后再进一步进行实验室诊断确诊病原。实验室诊断的方法主要包括病毒分离、反向间接血凝试验、中和试验、免疫组化试验、琼脂扩散试验。
1.8.1病毒分离
病毒分离是比较常规的方法,是众多试验室都不可缺少的技术之一。
使用此方法,需要提前准备9日龄SPF鸭胚若干,将获取病料与生理盐水1:1放入组织研磨器,将病料彻底研磨好后,导入1.5 m L离心管,用离心机9000 r/min离心5 min,用0.22 μm滤器过滤除菌后,将过滤液接种尿囊腔,将接种后的鸭胚放入培养箱孵育,观察6 d.并未发现胚胎死亡。取出尿囊液,可以进行电镜观察其形态结构。但是此方法,培养病毒周期过长,因为须要用到电镜观察,没有丰富的知识储备没有办法鉴别,而且电镜价格偏高且操作困难,对于基层人员培训困难所以不适合于基层推广和应用。
1.8.2反向间接血凝试验
反向间接血凝试验是一种可以快速鉴定抗原方法,间接血凝试验是可以检测抗体的方法。两种试验都是用于没有血凝性的病毒。间接血凝试验是将抗原和红细胞包被在一起,可以检测特异性抗体。如果有特异性抗体存在,抗原和抗体结合则使红细胞被动凝聚在一起。反向间接血凝试验则与间接血凝试验相反,反向间接血凝试验则是将抗体与醛化后的红细胞包被在一起,这样致敏的红细胞则可以和抗原特异性抗原结合,使红细胞发生特异性凝集。两种试验都是以红细胞为载体,将抗原或者抗体包被于红细胞表面。并不是所有红细胞都可以作为载体,最常见的是绵羊红细胞,用1%戊二醛将红细胞醛化,醛化后的红细胞可长期保存,不会溶血,且醛化后的红细胞对抗原或抗体的吸附能力较强。致敏用的抗原或抗体一般要求纯度较高,致敏抗原或者抗体有两种方法:第一种是在低PH、离子浓度的条件下抗原或者抗体可直接吸附在醛化后的绵羊红细胞上;另一种方法是间接法。这种方法让抗原或者抗体吸附在红细胞上则需要偶联剂,常用的偶联剂有两种分别是双耦氮联苯胺和氯化铬,耦氮联苯胺通过共价键使两者连接在一起。氯化铬则是通过金属阳离子静电的作用,使两者与醛化后的红细胞表面结合在一起。此方法经济方便、敏感性高、特异性强,也是一种比较方便、快捷检测特异性抗原和抗体的检测方法。用纯化过的新型鸭细小病毒抗体致敏醛化过后的红细胞,对鸭细小病毒阳性病料进行检测,且用其他的病毒测试致敏后的红细胞不会造成凝集,此方法具有准确性和特异性。
1.8.3中和试验
中和试验可以用于病毒鉴定、判定免疫血清中是否有抗体可以中和病毒的能力。将一定浓度的病毒与该病的抗体发生反应后,可以使该病毒丧失对鸭胚及其成纤维细胞致病能力的试验,称为中和试验。国内外学者针对检测GPV抗体,建立了病毒中和试验方法[62,63].
病毒中和试验的敏感性很高,操作方法简便。但该方法的弊端是所需胚体或细胞不易获得,试验重复性差。病毒在成纤维细胞上培养病毒需要在原代细胞上培养,不易传代、制作比较麻烦。要求细胞培养人员有很丰富的培养细胞经验,观察细胞是否有病变出现。并且检测周期时间较长,需要用到贵重的试验器材较多,只适合用于试验室研究用,不适于临床样品快速检测。
1.8.4免疫组化试验
免疫组化试验就是跟根据抗原和抗体会发生特异性结合的特性,通过标记物去标记特异性抗体或者二抗,带抗原或者抗体反应后,通过化学反应使标记物显色来确定组织是否含有特异型病毒或特异性病毒的含量。按标记物质的分类不同,可分为免疫荧光法、放射免疫法、酶标法等。
杨静红[64]用间接免疫组化方法检测攻毒后雏鹅体内不同时段、不同脏器的病毒含量在动物体内的分布情况。结果显示,感染后第1~21 d在心、肝、脾、肺、肾、胸腺、法氏囊各个肠段均能检测到病毒抗原。周春宇等[65]利用间接免疫组化试验对雏鹅新型病毒性肠炎病毒发病致死的雏鹅的各个组织进行检测结果呈阳性或强阳性。免疫组化试验的特异性非常高,主要是基于抗原和抗体的特异性结合,敏感性特别高,将抗体稀释上千倍,仍然可以和组织中的抗原发生特异性结合。
对病原在动物机体中的分布能精准定位,抗原和抗体反应后标记物会显色,可以明显的看到病原在组织中的分布。虽然此方法的准确度很高,但是由于做切片周期过长,不适合用于临时的检测,适用于试验室研究。
1.8.5琼脂扩散试验
琼脂扩散试验是血清学试验的一种,也是最常用的一种血清学实验。具有很高的特异性,操作简便的特点。它既可用来检测血清中的抗体,也可用来检测病料中抗原[66].郑美玉等[67]
利用琼脂扩散试验对鹅细小病毒进行了特异性检测,取得的效果良好。琼脂扩散试验是指特异性可溶性抗原和相对应的抗体在含有电解质的半固体凝胶中发生特异性沉淀,由于抗原抗体不断发生特异性结合不再扩散,在抗原抗体结合的部位形成肉眼沉淀线。用纯化过的鸭细小病毒的抗体与鸭细小病毒尿囊液可以形成特异性沉淀线,证明可以用此方法对该病毒做出检测。虽然该方法操作步骤少,实验耗材常见、操作简便适用于基层实验室推广和应用,但其反应结果受抗原抗体浓度和实验条件等因素影响,阳性检出率较低,反应灵敏度不高[68].
1.8.6聚合酶链式反应
聚合酶链式反应(Polymerase chain reaction, PCR)是近些年来比较热门的分子生物学检测技术,具有特异性高、敏感性高、方便快捷等优点,目前该技术已经在实验高度普及,称为检测病原主要方法之一。通过PCR仪可以在体外对某段特定基因片段进行扩增,使这段DNA片段大幅度增加,2~3个小时就可以对某些DNA片段扩增几百万倍,可以在病料病毒含量非常低的情况下,对病原进行准确鉴定。布日额[69]
2003年设计了一对鹅细小病毒的引物,目的是为了能准确鉴定出鹅细小病毒,设计这段引物是根据GPV H1株鹅细小病毒的VP1和VP3编码基因非重叠核苷酸序列,该引物可以准确的对鹅细小病毒做出检测,对鹅副粘病毒和鸭瘟无交叉反应,这一点证明了此实验具有也具有高度特异性。刘家森[70]
根据Gen Bank上番鸭细小病毒和鹅细小病毒基因序列差异分别设计了两对引物,为了检测这两对引物的特异性,分别用GPV、MDPV、DPV、DRV、CPV、FPLV的阳性病原进行测试引物的特异性,仅各自扩增出MDPV的目的片段和GPV的目的片段。其余结果都是阴性,证明此方法亦可用于番鸭细小病毒并且有高度的特异性。此方法的特异性和敏感性很高。
1.8.7套式聚合酶链式反应
套式PCR又称巢式PCR技术,是一种基于PCR技术改良的一种新的分子技术检测方法。巢式PCR技术在PCR扩增时,进行PCR时需要用两对引物,第一对引物进行PCR扩增片段时和普通的PCR没有什么区别,第二对引物称为巢式PCR,因为这段引物是在第一对PCR引物扩增的片段内部,第二段PCR扩增片段结合在第一对PCR扩增产物上,第二段PCR扩增片段短于第一段片段,这是巢式PCR技术和正常PCR技术不同的地方。由于套式PCR反应有两次PCR扩增,从而降低了扩增多个靶位点的可能性,因为样本与两套引物都互补的引物很少,增加了检测的敏感性,又有两对PCR引物与检测模板配对,增加了检测的可靠性。由于第二套位于第一轮PCR产物内部,而非目的片段包含两套引物结合位点的可能性极小,因此第二套引物不可能扩增非目的片段。这种巢式PCR扩增确保第二轮PCR产物几乎或者完全没有引物配对特异性不强造成非特异性扩增的污染。窦砚国等[71]
针对鸭细小病毒VP3基因设计了两对特异性引物,建立了检测鸭细小病毒的套式PCR检测方法,普通PCR的阳性检出率为26.7%,而套式PCR检测方法的为90%,并且该文献记载套式PCR比普通PCR技术的敏感性高1000倍,说明该方法具有良好的特异性和敏感性。
1.8.8实时荧光定量PCR技术
实时荧光定量PCR技术是将常规PCR与荧光化学物质相结合的检测技术。可高灵敏、高特异的对核酸进行定量分析。根据荧光化学物质与DNA结合的特异性可将其分为SYBR Green I染料法和Taq Man水解探针法。实时荧光定量PCR技术是近年来新出现的一种技术。该技术由普通PCR技术衍生而来,普通PCR扩增结束后需经过电泳染色和紫外分析仪显色处理才能观察结果,而且在开放的环境中对PCR产物进行分析,易造成假阳性,同时也不能对核酸准确定量,所以常规PCR技术比较繁琐。
SYBR Green I染料游离情况下仅可发出微弱光芒,但在DNA扩增时SYBR Green I非特异性的与双链DNA的小沟结合,从而发出强烈荧光;因为SYBR Green I染料和双链DNA的小沟结构是非特异性结合,因此容易受到非特异性扩增和引物二聚体的影响,使所得的定量结果并不可靠。所以其特异性不如探针法。
Taq Man水解探针法可特异性的与目的基因结合,其原理:主要是在PCR反应体系加入一个特异的荧光标记探针,根据荧光能量共振转移技术,当探针保持完整时,3\'
端的淬灭基团抵消了5‘端发射基团的荧光发射,这时检测不到荧光信号。在PCR的退火期,探针与模板发生特异性杂交,当延伸期引物在Taq酶作用下沿DNA模板延伸到探针位置,由于所用Taq酶具有5’→3‘外切活性,发生置换反应,使5’端标记荧光发射基团FAM(6-羧基荧光素)与3‘端标记荧光淬灭基团TAMRA(6-羧基四甲基若丹明)分离,荧光信号得到释放,这时荧光探测系统就能检测到光密度的增加。模板每复制1次,就有1个探针被切断,伴随着1个荧光信号被释放。由于理论上被释放的荧光基团数和PCR产物数是一对一的关系,因此,可根据PCR反应液中的荧光强度即可计算出初始模板的数量[72].
1.9预防
2014年此病在首次在大陆发生大面积流行。因此本病的发生时间较短,对此病的治疗措施很薄弱,且该病的治愈率很低,就算患病鸭痊愈后,也变成了僵鸭,没有养殖价值,因此应及早从预防着手。预防主要从两方面入手,一方面是生物安全,另一方面用疫苗进行防治。
1.9.1生物安全措施
首先,养殖场首先保持自身鸭场的纯净性,生产上采购鸭苗或售出成品鸭尽量采取全进全出,尽量将隔离、消毒工作做好,外来的车辆、人员、饲料和用具都进行消毒。定期对鸭场进行消毒,将场内病原杀灭干净,患病鸭的粪便和病死鸭的尸体都要进行无害化处理。加强鸭场的饲养管理,提高鸭群的抵抗力。防寒保暖,尽量保持到鸭子适宜的环境[72].
1.9.2疫苗防控
由于市场上没有该病的成品疫苗,且患病的动物的治疗价值很低,因此对该病的控制还主要用疫苗进行防控,还需加快对该病研制成品疫苗的步伐。
1.10技术路线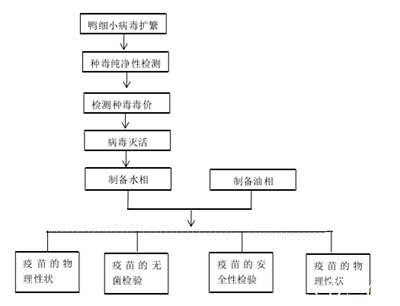
1.11研究目的和意义
新型鸭细小病毒是从小鹅瘟变异而来的一种新型病毒,这种病毒造成的病称为鸭短喙侏儒综合征。
此病在2014年以前,在大陆没有发生过大面积的流行。该病的突然爆发给我国养鸭业造成极大的经济损失。该病毒只感染10~25日龄的雏鸭,成年鸭对此病并不敏感。该病对雏鸭造成的危害并不是大批量的死亡,而是造成生长障碍,导致肉鸭出栏率降低。治愈后,也变成了没有培养价值的僵鸭。所以提前用疫苗进行免疫变成了特别重要的免疫程序。因为本病发现时间较短,并且市场上并没有有效防治本病的疫苗。因此,本研究针对这一现象,研发了一款用于预防新型鸭细小病毒的油乳剂灭活疫苗,有效遏制该病肆无忌惮的蔓延。



